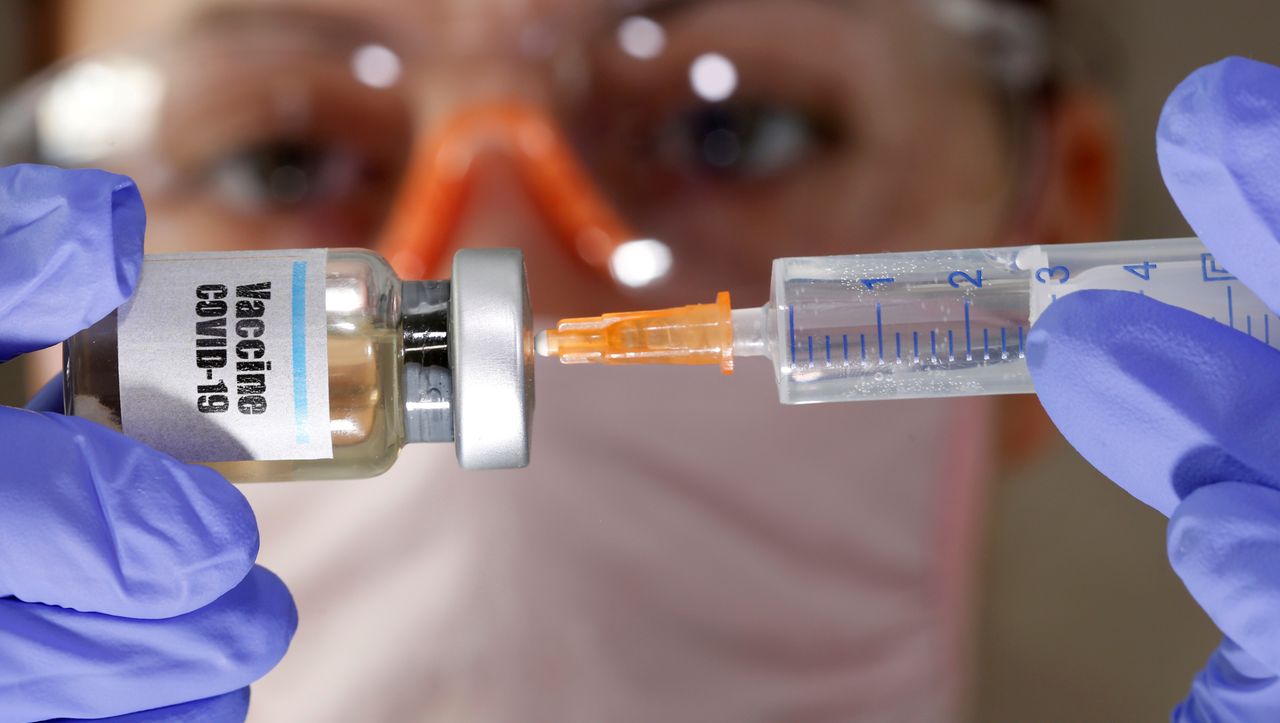
Einen Tag nach dem amerikanischen Unternehmen Moderna folgt nun auch Biontech: Mit seinem amerikanischen Partner Pfizer startet das Mainzer Biopharma-Unternehmen eine neue Testphase für einen Impfstoffkandidaten. „Heute starten wir unsere globale Studie, an der bis zu 30.000 Teilnehmer teilnehmen werden“, sagte Ugion Sahin, CEO von Biontech.
Die klinische Phase II / III-Studie sollte unter anderem zeigen, ob der Wirkstoff BNT162b2 tatsächlich vor einer Infektion mit Sars-CoV-2 schützt. In einem ähnlich fortgeschrittenen Teststadium, so eine Überprüfung der WHO Derzeit nur vier weitere Projekte.
Der amerikanische Hersteller hatte es erst am Montag Moderna gibt den Beginn seiner Phase-III-Studie bekannt. Die ersten Ergebnisse sind möglicherweise im November verfügbar. Bisher wurde gezeigt, dass mehrere Impfstoffkandidaten die Immunantwort verstärken. Es gibt jedoch immer noch Hinweise darauf, dass eines der Mittel wirklich schützt.
Biontech- und Pfizer-Tests werden an Probanden im Alter zwischen 18 und 85 Jahren in 120 Studienzentren weltweit, einschließlich Deutschland, durchgeführt. Wenn die Studie erfolgreich ist, werden Pfizer und Biontech bereits im Oktober 2020 das Zulassungsverfahren beantragen und, falls genehmigt, bis Ende des Jahres bis zu 100 Millionen Impfstoffdosen und bis Ende 2021 mehr als eine Impfdosis produzieren. 0,3 Milliarden Impfstoffdosen.
Sowohl der Moderna-Kandidat als auch der Biontech-Wirkstoff sind sogenannte RNA-Impfstoffe und enthalten genetische Informationen über den Erreger. Mit ihrer Hilfe sollten die Körperzellen der geimpften Probanden Oberflächenproteine des Coronavirus produzieren – auf die das Immunsystem reagiert. Es wurde jedoch noch kein Impfstoff für Menschen zugelassen, der auf dieser Technologie basiert.
Bisher wurde der Wirkstoff an ca. 120 Probanden getestet. Biontech und Pfizer sprachen von einem „vorteilhaften allgemeinen Toleranzprofil“. Nebenwirkungen wie Fieber, Müdigkeit und Schüttelfrost waren nur leicht bis mittelschwer und klangen nach ein oder zwei Tagen ab.
Um die Forschung weiter zu finanzieren, sammelte Biontech mit einer Kapitalerhöhung über eine halbe Milliarde Dollar. Biontech und Pfizer haben die Vereinigten Staaten ursprünglich zu 100 Millionen Impfstoffdosen verpflichtetwenn das Produkt zugelassen wird. In diesem Fall werden bis zu 500 Millionen zusätzliche Dosen als optionale Nachbestellung versprochen. Es gibt auch eine erste Liefervereinbarung mit Großbritannien.

Freiberuflicher Alkoholiker. Begeisterter Webfanatiker. Subtil charmanter Zombie-Junkie. Ergebener Leser.
You may also like
-
Graz in Österreich testet intelligente Verkehrssensoren von LMT / Artikel
-
Bosnien sucht österreichische Unterstützung für Frontex-Statusabkommen – EURACTIV.com
-
Die österreichische Zentralbank senkt die BIP-Wachstumsprognose für 2016 und 2017
-
Österreich verabschiedet Resolution, die Holodomor in der Ukraine als „entsetzliches Verbrechen“ bezeichnet; Russland reagiert
-
Die österreichische Zentralbank prognostiziert für 2023 eine leichte Rezession und dann ein Wachstum von 0,6 %